Non-associativ immunmedieret hæmolytisk anæmi (IMHA) er en ikke helt ualmindelig forekommende årsag til svær regenerativ anæmi hos hund. Sygdommen kan have store konsekvenser for patienten både med henblik på co-morbiditeter, men også i forhold til overlevelse1,2. I ca. 30 % af tilfældene vil anæmien være vedvarende non-regenerativ, og sygdommen kan betegnes som en non-regenerativ immunmedieret anæmi (nrIMA)3–5 eller precursor-targeted immune-mediated anemia (PIMA)6–8. I denne artikel bruges betegnelsen nrIMA.
Midaldrende steriliserede tæver af racerne whippet, miniature gravhund, boxer og greyhoundblandinger er prædisponerede for nrIMA3, og der ses en høj forekomst af gravhunde i populationer med nrIMA4,7,8. Den non-regenerative anæmi opstår som følge af et immunmedieret angreb, der typisk vil være rettet mod de erytroide forstadier i knoglemarven. Herved kan eventuel hæmolyse, spherocytose, autoagglutination og positiv direkte anti-erytrocyt antistof test (Coombs test®) være fraværende ved nrIMA3,4,7,9.
Det er en udfordring at behandle nrIMA, da der trods immunsupprimerende terapi kun ses en overlevelse på ca. 60 % efter 3 måneder3,5,7, og cirka en tredjedel af hundene, som opnår et regenerativt respons, vil få recidiv3. Samtidigt kan responset på behandlingen være forsinket, idet der kan gå flere uger til måneder, før der ses tegn på regeneration i blodbilledet3,4,7. I nogle tilfælde kan det være nødvendigt med administration af flere immunsuppressive medikamenter i kombination for at opnå remission af sygdommen, hvilket kan øge risikoen for bivirkninger.
Denne artikel beskriver en case med nrIMA og berører de diagnostiske og terapeutiske problemstillinger, der følger med sygdommen.
Casepræsentation
En 5 år gammel intakt tæve af racen gravhund blev præsenteret hos egen dyrlæge. Ejer havde bemærket, at hunden virkede meget stille, nedstemt og træt, hvilket havde stået på nogle dage. Hunden havde opholdt sig i Danmark uden rejseaktivitet til udlandet og var fuldt vaccineret, ormebehandlet og havde modtaget regelmæssig flåtprofylakse. Intet i anamnesen indikerede, at hunden havde været eksponeret for toksiner eller andre medikamenter, der kunne udløse en immunmedieret anæmi. Ved den kliniske undersøgelse blev der fundet blege slimhinder, ellers var resten af undersøgelsen upåfaldende.
Diagnostik
Den initielle minimumsdatabase (hæmatologi, biokemi og urinanalyse) identificerede en moderat normokrom og normocytær non-regenerativ anæmi med hæmatokrit (hct) på 23,9 %. Leukocyt- og trombocyttallene var indenfor referenceintervallerne. Den biokemiske profil og urinanalysen var upåfaldende uden tegn på bilirubinæmi/-uri eller hæmoglobinuri.
Serologiske undersøgelser for vektorbårne sygdomme var negative for Anaplasma phagocytophilum[i], Anaplasma platys, Borrelia burgdorferi, Ehrlichia canis, Ehrlichia ewingii, Dirofilaria immitis og Angiostrongylus vasorum[ii]. En videre undersøgelse med polymerase chain reaction for Anaplasma spp. var negativ. Der blev desuden foretaget en abdominal ultralydsscanning og taget thorax-røntgen i 3 planer, hvor der ikke blev fundet underliggende sygdomme. På baggrund af de kliniske fund blev en autoimmun lidelse mistænkt, og immunsuppressiv behandling blev opstartet.
Efter 5 dages behandling blev der udført en Coombs test®, som var negativ. Anæmien og de kliniske tegn blev forværrede med udvikling af tachypnø og auskultation af en holosystolisk mislyd grad 3/6 på dag 11. Hunden blev henvist til blodtransfusion, knoglemarvsbioptering og -aspiration.
Initial hæmatologi hos henvisningsdyrlægen viste en svær persisterende non-regenerativ anæmi med en hct på 14,2 % (ref. 37,3-61,7 %) og et absolut reticulocyttal på 15.600/µL (ref. 10-110.000/µL) (tabel 1). På baggrund af tallene blev den korrigerede reticulocyt procent (KR%) og reticulocyt produktions indeks (RPI) beregnet for bedre at kunne estimere det regenerative respons. Værdien for KR% blev beregnet til 0,3 % (regenerativt respons > 1 %) og RPI blev beregnet til 0,13 (regenerativt respons > 1)[iii].

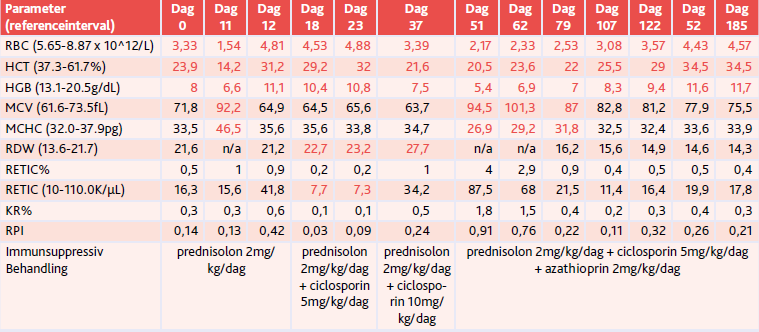
Tabel 1. Udvalgte hæmatologiske parametre i forhold til den administrerede immunsuppressive protokol. Den røde farve angiver værdier udenfor referenceintervallet. RBC, red blood cell; HCT, hæmatokrit; HBG, hæmoglobin; MCV, mean cell volumen; MCHC, mean corpuscular haemoglobin; RDW, red blood cell distribution width; RETIC%, reticulocyt procent; Retic, reticulocyttal; KR%, korrigerede reticulocyt procent (regenerativ respons > 1 %); RPI, reticulocyt produktions indeks (regenerativt respons > 1); n/a, non-applicable.
I blodudstrygningen blev der kun fundet få reticulocytter og metarubricytter, hvilket kunne bekræfte, at hundens anæmi var non-regenerativ. Yderligere blev der fundet et stort antal spherocytter (≥ 5 spherocytter pr. hpf) og elliptocytter samt enkelte ghost-celler (billede 1) En saltvandsagglutinationstest (1:4 fortyndning) var negativ for autoagglutination. Knoglemarvsbiopsi og -aspirater taget fra proximale humerus viste en erythroid hyperplasi domineret af sene erytroide forstadier, men et forholdsvist lavt antal reticulocytter. Desuden blev der fundet fagocyterede sene erytroide forstadier af makrofager (rubrifagocytose), og der var mistanke om myelofibrose. Der var komplet modning og normoplasi af de myeloide, lymfoide og megakaryocytære cellelinjer, og der blev ikke fundet tegn på infektiøse agens eller neoplasi.
______
[i] SNAP 4DX PLUS Test, IDEXX laboratories, westbrook, Maine, USA
[ii] Angio DetectTM Test, IDEXX laboratories, westbrook, Maine, USA
[iii] Der henvises til formlerne på hjemmesiden https://eclinpath.com/hematology/anemia/assessment-regeneration/ brugt til udregning af KR% og RPI

Billede 1. Billedet viser monolaget fra blodudstrygningen udført på dag 11. Der ses et signifikant forøget antal spherocytter (markeret med pile) og elliptocytter (markeret med asterisk).

Figur 1. Viser værdier for hundens hæmatokrit mellem dag 0-185 i forhold til ændringer i den immunsuppressive protokol. Det skraverede felt angiver referenceintervallet for hæmatokrit. De vertikale stiplede linjer, markeret med bogstaverne A, B, C og D, angiver behandlingsændringer. Dag 0 til A: Prednisolon 2 mg/kg/dag; A til B: Prednisolon 2 mg/kg/dag + ciclosporin 5 mg/kg/dag; B til C: Prednisolon 2 mg/kg SID + ciclosporin 10 mg/kg/dag*; C til dag 185: Prednisolon 2 mg/kg/dag + ciclosporin 5 mg/kg/dag + azathioprin 2 mg/kg/dag. *Ciclosporin dosis blev reduceret fra 10 til 5 mg/kg/dag fra dag 48 på grund af bivirkninger.
Terapi og efterfølgende forløb
Behandling med prednisolon (2 mg/kg/dag)[i] og omeprazol (2 mg/kg/dag)[ii] blev opstartet i forbindelse med det første dyrlægebesøg. For at stabilisere patienten til den videre udredning med knoglemarvsundersøgelsen blev der på dag 11 administreret en blodtransfusion med 434 ml fuldblod (DEA 1.1 negativ, hct 44 %). Før transfusionen blev der udført uforligelighedstests imellem donor og recipient i form af cross-matching og blodtypebestemmelse. Recipienten var blodtype DEA 1.1 positiv. Transfusionen blev administreret indenfor 4 timer med en rate på 0,25-10ml/kg/time. Der blev ikke observeret transfusionsreaktioner, og dagen efter var recipientens hct steget til 31,2 %.
Da resultatet på knoglemarvsprøverne forelå på dag 18, blev adjuverende immunmodulerende behandling med lav dosis ciclosporin (5 mg/kg/dag)[iii] og antitrombotisk profylakse med clopridogrel (2 mg/kg/dag)[iv] koblet på protokollen af henvisningsdyrlægen. Der blev administreret en lav dosis ciclosporin (5 mg/kg/dag) initelt, som efterfølgende blev øget til 10 mg/kg/dag fra dag 37 på grund af et utilfredsstillende respons på behandlingen (figur 1).
Desværre udviklede hunden bivirkninger i form af anoreksi, kvalme, vomitus og diarre på den forøgede dosis, så dosis blev reduceret til 5mg/kg/dag fra dag 48. Adjuverende immunmodulerende behandling med azathioprin (2 mg/kg/dag)[v] blev koblet på protokollen fra dag 51. På de efterfølgende blodprøvekontroller blev der observeret en langsomt stigende hct uden andre synlige tegn på regeneration i blodbilledet.
Værdierne for det absolutte reticulocyttal svingede henholdsvis imellem 7.700-87.500/µL (ref. 10-110.000/µL) fra behandlingsstarten og indtil komplet remission blev observeret. Tilsvarende lå RPI < 1 og KR% < 1 % på de fleste analyser, hvor anæmien kunne karakteriseres som makrocytær og hypo- eller normokrom. En blodudstrygning fra dag 62 viste nu kun få spherocytter, og der var ingen synlige spherocytter på blodudstrygningen fra dag 122.
Efter 185 dages behandling blev udtrapningen i den immunsuppressive protokol påbegyndt, da hct havde ligget stabilt over 30 % gennem flere uger. På dette tidspunkt var flere af leverparametrene forhøjede med alanin aminotransferase på 185 (ref. 10-125) og alkalisk fosfatase på 617 (ref. 23-212).
Hunden udviklede efterfølgende en absces i huden på venstre maxil. Denne responderede på behandling med clindamycin (11 mg/kg/dag)[vi]. Leverparametrene normaliserede sig samtidigt med nedtrapningen af de immunsupprimerende farmaka. Behandlingen blev helt seponeret efter 13 måneder, hvor hct var indenfor referenceintervallet.
______
[i] Prednicortone Vet. Tabletter 5mg, Dechra Veterinary Products A/S, Uldum, Danmark
[ii] Omestad. Tabletter 10mg, STADA Arzneimittel AG, Tyskland
[iii] Sporimune Vet. Oral opløsning 50mg/ml, Dechra Veterinary Products A/S, Uldum, Danmark
[iv] Clopridogrel Actavis. Tabletter 75mg, Balkanpharma Dupnitsa AD, Bulgarien
[v] Imurel. Tabletter 25mg, Excella GmbH & Co. KG, Tyskland
[vi] Antirobe Vet. Tabletter 25mg, Zoetis Animal Health Aps, København, Danmark
Diagnosen nrlMA blev bekræftet ved knoglemarvsundersøgelser.
Diskussion
Udviklingen af den persisterende non-regenerative anæmi kunne hos denne patient forklares ud fra et bredt immunologisk angreb rettet mod; 1) det sene erytroide forstadie; 2) reticulocyt stadiet; og 3) den modne erythrocyt. Diagnosen blev endeligt baseret på knoglemarvsfund af rubrifagocytose og erytroid hyperplasi bestående primært af forstadier, men med et forholdsvist lavt antal reticulocytter (tegn på modningsarrest). Desuden blev der fundet markant spherocytose i blodudstrygningen på dag 11, som gradvist forsvandt på de efterfølgende kontrolblodprøver i behandlingsforløbet. Hverken saltvandsagglutinationstesten eller Coombs test® kunne bekræfte en immunmedieret årsagssammenhæng, men dette er ikke ualmindeligt. Testene er baseret på at kunne detektere tilstedeværelsen af IgG og IgM anti-erytrocyt antistoffer samt eventuelt komplement C3 hos patienter med IMHA. Coombs test®, baseret på forskellige assays, er rapporteret til at have en sensitivitet imellem 61-82 % og en specificitet imellem 94-100 % for IMHA9.
Saltvandsagglutinationstesten udført i en 1:4 fortynding har i flere studier vist en sensitivitet imellem 84-88 % og en specificitet imellem 49-100 % for IMHA9,10. Der kan altså forekomme falsk negative tests, men allerede påbegyndt glucokortikoid behandling kan også have påvirket testene i denne case. Observationen af et immunmedieret angreb rettet mod erytrocytterne i kredsløbet er et variabelt fund ved nrIMA, og dette kan give overlap med IMHA. I to undersøgelser opfyldte 57 %-59 % af hundene med nrIMA mindst et kriterium (spherocytose, autoagglutionation, positiv Coombs test, hæmolyse) for IMHA3,4. I modsætning til dette blev positiv Coombs test® eller spherocytose kun fundet hos henholdsvis 0-22 % og 0-3 % af hundene med nrIMA i tre andre studier 6,7,11.
Der er endnu ikke tydelig evidens på, at det vil have betydning for behandlingsresponset eller prognosen, når hunde med nrIMA viser tegn på perifær destruktion af erytrocytter. Et studie fra 2000 viste ingen sammenhæng imellem Coombs test® resultater eller spherocytose i forhold til, om hunde responderede på en given behandling eller ej4. Et andet studie fra 2021 viste, at hyperbilirubinæmi - en potentiel indikator for hæmolyse - ikke havde prognostisk værdi i forhold til overlevelsen hos nrIMA patienter3.
Udtagelse af knoglemarvsaspiration og -biopsier er central i udredningen af nrIMA i forhold til at bekræfte det immunmedierede angreb i knoglemarven og udelukke underliggende intramedullære sygdomme, som kan resultere i ineffektiv erytropoiese eller udløse nrIMA såsom neoplasi, dysmyelopoiesis, hæmofagocytisk syndrom, nekrose, myelofibrose, »pure red cell aplasia« og jernmangel. Fundet af rubrifagocytose er vigtigt i forhold til at bekræfte et immunmedieret angreb på knoglemarvens erytroide forstadier. Fundet betragtes som værende diagnostisk for nrIMA, hvis der kan dokumenteres en non-regenerativ anæmi af minimum 5 dages varighed, og underliggende sygdomme er udelukkede i den diagnostiske proces3,7.
Erytroid hyperplasi med modningsarrest og rubrifagocytose vil være de mest karakteristiske fund for nrIMA, da det ses hos henholdsvis 56-62 % og 90-92 % af patienterne 3,4,7. Rubrifagocytosen kan være fraværende hos nogle hunde med nrIMA, hvor der kun ses tegn på modningsarrest, og her er grundlaget for diagnosen mere usikker3,7
Der var mistanke til myelofibrose ud fra knoglemarvsprøverne, og dette kunne forklare det morfologiske fund af elliptocytter set i blodudstrygningen initelt. Forskellige former for knoglemarvspatologi, som myelofibrose, dysmyelopoiesis, nekrose, blødning og ødem er dokumenteret hos patienter med nrIMA3–5,7. De knoglemarvspatologiske fund er blevet mistænkt for at kunne bidrage til den ineffektive erytropoiese sammen med den immunmedierede destruktion af erytroide forstadier og erytrocytter. Dog er sandsynligheden for overlevelse og tid til opnåelse af et regenerativt respons ikke associeret med knoglemarvsfund eller sværhedsgraden af myelofibrose3,7.
Der findes ikke konsensusretningslinjer for immunsuppressiv behandling af nrIMA som ved IMHA. Det kan give usikkerheder i beslutningsprocessen omkring valg af medikamenter, dosis, frekvens og administrationslængde. Kun ét studie har rapporteret brug af en standardiseret protokol i behandlingen af nrIMA, hvor prednisolon (2mg/kg/dag) og ciclosporin (10mg/kg SID) blev administreret i 8 uger11.
Der findes ikke konsensusretningslinjer for immunsuppressiv behandling af nrIMA som ved IMHA.
Hvis behandlingen ikke havde effekt, blev ciclosporin udskiftet med mycophenolat mofetil (30mg/kg/dag) i 8 uger. Ud af 11 hunde responderede 7 på den første protokol og 1 responderede på den anden protokol11. Responsraten og tid til opnåelse af et respons var dog ikke bedre, end hvad der tidligere er rapporteret for nrIMA ved brug af andre behandlingsprotokoller3,4,7. I tilfældet her responderede hunden først efter 62 dage på en kombination af prednisolon, ciclosporin og azathioprin, med normalisering af hæmatokrit efter 185 dage. Observationerne korrelerer med andre studier, som har rapporteret immunsuppressiv behandling med en langsom median responstid på cirka 1 måned, hvoraf nogle patienter først viste tegn på regeneration efter cirka 3-4 måneders behandling3,7,11. Prednisolon i kombination med adjuverende ciclosporin eller azathioprin var de hyppigst anvendte kombinationer, hvor færre blev behandlet med prednisolon alene3,4,6,7,11. Hos en minoritet af patienterne var behandling med alle tre medikamenter nødvendigt for at opnå et regenerativt respons3,6,7.
Beslutningen om at bruge alle tre medikamenter i dette tilfælde blev baseret på det manglende respons. Dog foreligger der ikke evidens for opnåelse af en bedre effekt ved brugen af mere end to immunsuppressive medikamenter, og risikoen for alvorlige bivirkninger kan være forøget12. Det kunne have været en overvejelse at substituere ciclosporin med azathioprin i protokollen hos denne patient, da der så ud til at være en begrænset effekt af kombinationen med prednisolon og ciclosporin. På den højere dosis ciclosporin (10mg/kg/dag) blev der observeret gastrointestinale bivirkninger hos hunden, og dosis måtte derfor nedjusteres. Disse bivirkninger er en kendt komplikation til ciclosporin behandling13,14. Et studie beskrev muligheden for at starte med en lav dosis ciclosporin (5mg/kg/dag) i kombination med prednisolon og gradvist øge dosis til 10mg/kg/dag indenfor en 14 dages periode i forhold til at reducere incidensen af bivirkninger11. Til trods for denne tilgang udviklede 2 ud af 11 hunde gastrointestinale bivirkninger relateret til ciclosporin behandlingen. Men i samme studie responderede en enkelt hund på den lave dosis af ciclosporin (6mg/kg/dag), og derfor kunne det være en overvejelse gradvist at øge ciclosporin dosis over en kortere periode hos patienter med nrIMA, hvis anæmien udvikler sig langsomt.
Selvom den valgte kombination af prednisolon, ciclosporin og azathioprin resulterede i et regenerativt respons hos hunden, blev der set parakliniske tegn på hepatotoksicitet. Desuden udviklede hunden en absces, som ophelede ved udtrapning af de immunsupprimerede farmaka og ved behandling med antibiose. Hepatotoksicitet er både beskrevet som en mulig komplikation til ciclosporin- og azathioprin-behandling, og nogle hunde får påvirkning af leverenzymer under glukokortikoid terapi14. Vedvarende stigninger i levertal eller tegn på opportunistiske infektioner bør føre til overvejelser i forhold til behandlingsprotokollens sammensætning og mulighed for nedtrapning bør overvejes. Udviklingen af abscessen kan i dette tilfælde også skyldes det forhalede behandlingsrespons, der ses ved nrIMA, som øger risikoen for infektionssygdomme pga. den langvarige immunsuppression.
Hos denne patient var det svært at vurdere, om behandlingen var ineffektiv, eller om mere tid var nødvendig i forhold til at opnå et respons. Dette skyldes, at der ikke findes systemiske markører for sygdomsaktiviteten i knoglemarven, hvorved indirekte markører såsom vurdering af hct eller reticulocytose er eneste indikatorer for, om patienter med nrIMA responderer. Der blev ikke identificeret tegn på regeneration i hundens perifere blodbillede i forbindelse med, at hæmatokritten steg, men spherocytosen kunne ikke længere erkendes på kontrolblodudstrygningerne, hvilket indikerede en dæmpning af immunsystemet. Normalt vil reticulocyt parametre (absolutte reticulocyttal, KR%, RPI) eller vurdering af en blodudstrygning igennem fund af polykromasi og anisocytose kunne hjælpe med et identificere, om en anæmi er non-regenerativ eller regenerativ 15,16. Man kunne mistænke en langsom modning og frigivelse af erytroide forstadier til kredsløbet som forklaring på de manglende tegn på regeneration i dette tilfælde.
Denne hund med nrIMA gik i komplet remission og er vendt tilbage til et normalt liv uden tegn på sygdomsrecidiv cirka 3 måneder efter endt terapi. Dette korrelerer med to nyere studier, hvor hovedparten af hundene opnåede et regenerativt respons på immunsuppressiv behandling3,11. Dog rapporterede det ene studie en overlevelse på 60 % ved 3 måneder og 40 % ved 12 måneder efter, at diagnosen blev stillet3.
Til sammenligning har flere studier rapporteret overlevelsesrate mellem 30-70 % for IMHA2,17,18. Den nedsatte overlevelsesrate for nrIMA kan måske forklares ud fra det langsomme behandlingsrespons eller udviklingen af recidiv, som får nogle ejere til at vælge aflivning frem for at fortsætte behandlingen.
Konklusion
Denne case viste, at nrIMA er en autoimmun sygdom, som kan have et diagnostisk overlap med IMHA. Identifikationen af en erytroid hyperplasi med modningsarrest og rubrifagocytose i knoglemarven var diagnostisk for nrIMA hos denne patient. Tegn på erytroid regeneration blev først opnået efter 62 dage på immunsuppressiv behandling. Hæmatokritten blev normaliseret efter 185 dages terapi, og hunden blev senere erklæret rask, selvom den anvendte immunsuppressive protokol var associeret med bivirkninger. Regelmæssig og langvarig monitorering må påregnes ved nrIMA i forhold til vurdering af det regenerative respons og for at minimere risikoen for udviklingen af alvorlige bivirkninger på den immunsuppressive behandling.





