Babesiose er en flåtbåren parasitsygdom, der skyldes infektion med protozoen Babesia. Babesia-slægten omfatter over 100 arter, som er infektive for vilde dyr såvel som domesticerede. Dog er babesiose globalt bedst kendt som en kvægsygdom. Udover at være en velkendt kvæg-parasit, er Babesia i stigende grad også anerkendt som en zoonose. I Europa er der dog kun rapporteret få tilfælde af human babesiose, herunder et alvorligt tilfælde i Norge i 20151 og et fatalt tilfælde i Finland i 20102.
Hos kvæg derimod er babesiose en alvorlig og vidt udbredt sygdom. I Europa forekommer fire Babesia-arter hos kvæg: B. bigemina, B. bovis, B. divergens og B. major3, hvoraf B. divergens er den hyppigste årsag til bovin babesiose i Nordeuropa4 , og den er zoonotisk. Babesia overføres mellem modtagelige værter med flåter af slægten Ixodes, dog har de enkelte Babesia-arter forskellige flåt-arter som vektor, hvorfor udbredelsen af Babesia-arter hænger sammen med udbredelsen af den tilhørende flåt-art.
Babesia divergens benytter næsten udelukkende skovflåten Ixodes ricinus (Fig. 1), som er vidt udbredt i Europa, herunder hele Danmark5. DTU Veterinærinstituttet har undersøgt et større antal danske skovflåter for Babesia-infektion. Flåterne var indsamlet fra 24 forskellige områder i Danmark med skov og eng fra både Sjælland og Jylland. Babesia divergens-positive flåter blev identificeret fra i alt ni områder og forekom både i Jylland og på Sjælland.
Skovflåten foretrækker områder med høj jordbundsfugtighed, da den er sensitiv for udtørring. Risikoen for flåtbid og dermed Babesia-infektion er derfor større i områder med buskads, træer og græs (Fig. 2). Velafgræssede indhegninger med direkte sol og uden buskads er derimod ikke optimale levesteder for skovflåter. Findes der enkelte træer på en afgræsset mark, kan det dog i visse tilfælde være et hotspot for skovflåter. Den globale opvarmning i form af mildere vintre samt habitatforandringer kan muligvis føre til længere perioder med flåtaktivitet og øget antal flåter, hvilket kan betyde øget risiko for Babesia-infektioner.
Livscyklus
Skovflåtens livscyklus består af tre udviklingsstadier: Larver, nymfer samt voksne hanner og hunner. Udviklingen fra æg til voksen tager ca. 3 år. I hvert stadie har flåten brug for ét blodmåltid (på nær hannens tredje stadie), og det lader til, at alle stadier kan overføre B. divergens. Larverne får typisk deres første blodmåltid fra små pattedyr, såsom gnavere. Herefter udvikler de sig til nymfer og har brug for endnu et blodmåltid, igen fra små pattedyr. Efter andet blodmåltid udvikler nymferne sig til voksne flåter, og hunflåten tager et blodmåltid på et større pattedyr fx kvæg.
Når en skovflåt indtager et blodmåltid fra en inficeret vært, vil Babesia-inficerede erytrocytter blive suget med op. Herefter vandrer parasitten over i flåtens spytkirtler, hvor den formerer sig, og bliver overført ved flåtens næste blodmåltid som sporozoitter (det infektive stadie). Babesia divergens kan også overføres transovarialt6. Dette sker ved, at parasitten trænger ind i hunnens æg, hvor nye infektive sporozoitter udvikles gennem en række delingsstadier. Denne form for transovarial overførsel kan resultere i et stort antal inficerede flåter. Da infektionen persisterer i flåterne gennem deres forskellige udviklingsstadier samt overføres fra hun til afkom, kan Babesia-infektionen opretholdes i flåtpopulationen uden tilstedeværelse af inficerede værter i op til fire år7.
Efter overførsel af sporozoitter fra vektor til vært, trænger sporozoitterne ind i erytrocytterne (Fig. 3), hvorefter de kaldes trophozoitter. Trophozoitterne deler sig ved binær fission og producerer to datterceller, kaldet merozoitter. Merozoitterne frigives fra erytrocytterne til blodstrømmen, ved at cellerne brister, hvorefter nye erytrocytter inficeres. Merozoitterne fortsætter med at formere sig og invadere nye erytrocytter, indtil værten enten dør, bliver behandlet, eller indtil immunsystemet hindrer yderligere deling. En lille andel af parasitterne omdannes dog til ikke-delelige gamonter, som bliver inde i erytrocytterne og venter på at blive overført til den næste flåt i forbindelse med et blodmåltid4.

Figur 3. Udstrygningspræparat af Babesia divergens (sort pil) i erytrocytter fra Limousinekvæg fra Samsø.
Babesiose-sygdomsforekomsten er typisk bimodal sæsonfordelt med en forårsepidemi i april til juni og en efterårsepidemi fra august til oktober. Tidspunktet for forårsepidemien afhænger dog af temperaturen i foråret4. Babesiose forårsaget af B. divergens kan variere fra en mild subklinisk infektion til en alvorlig livstruende tilstand med akut feber, anæmi, anoreksi, depression, øget respiration og puls samt det helt karakteristiske blod i urinen, hvorfor infektionen også er kendt som blodpis eller »redwater«4. Anæmi, hæmaturi og feber forårsages af destruktionen af erytrocytter i forbindelse med opformeringen af merozoitterne. Dette kan i nogle tilfælde forløbe perakut, og dyret dør få dage efter infektion, men det typiske forløb medfører akutte symptomer 1-2 uger efter infektion.
Tabsvoldende sygdom
Udbrud af sygdommen i en kvægbesætning kan medføre alvorlige tab som følge af øget mortalitet, aborter, fald i kød- og mælkeproduktionen samt omkostninger til kontrol og behandling. En interessant og muligvis unik kendsgerning ved bovin babesiose er, at sværhedsgraden af kliniske symptomer samt mortaliteten er omvendt relateret til alder. Dvs. at smittet ungkvæg (< 9 måneder) sjældent udviser kliniske symptomer. Dette hænger muligvis sammen med en medfødt immunitet mod bovin babesiose, samt at antistoffer overføres fra koen til kalven via colostrum3, hvorfor kalve, der inficeres i løbet af de første 10-12 levemåneder, vil udvikle immunitet overfor Babesia og dermed fungere som reservoirværter uden nævneværdige kliniske symptomer. Smitten kan derved opretholdes i et område uden tilstedeværels af kliniske tegn, fordi kalve opvokset i endemiske babesiose-områder typisk ikke vil udvikle babesiose som voksne. Derimod vil naive dyr, som flyttes fra et område uden Babesia til et endemisk Babesia-område, have stor risiko for udvikling af babesiose.
Historisk babesiose-overblik fra Samsø og Stavns fjord
Afgræsningen på Hjorteholm i Stavns fjord ved Samsø (Fig. 4) begyndte i nyere tid i 1975, hvor ca. 70 kreaturer fra forskellige besætninger, både malkekvæg og Herefordkvæg, blev sejlet over til øen. Malkekvæget var 1-årskvier, mens Herefordkvæget primært var køer med kalve. Kreaturerne blev sejlet over i joller (Fig. 5), hvilket gerne tiltrak sig en del opmærksomhed fra turister og lokale.
Dyrlæge Niels Henrik Roug har været praktiserende dyrlæge på øerne siden 1977 og kan berette om en unik 40-årshistorie om babesiose på disse øer. Dyrlæge Roug fortæller, at i 1977, da han etablerede sig som dyrlæge, havde babesiose så vidt han vidste aldrig været diagnosticeret på øerne. Ligeledes var der de første 2-3 år efter 1975 heller ingen udbrud af babesiose på Hjortholm. Derefter observerede man enkelte døde kreaturer i ny og næ. Det levede man ligesom med, da det var vanskeligt at se det kliniske billede med blod i urin, til trods for at der blev gjort et forsøg. Dyrene blev ofte først fundet efter at have ligget døde et par dage.
I 1985 ankom to nye besætninger af Charolaisracen. Blandt disse dyr var der også dødsfald, men her var man heldig at finde et klinisk tilfælde med blodpis og svær anæmi, der havde lagt sig på brystet. Hermed kunne babesiose diagnosticeres, og koen få den rette behandling. Koen blev succesfuldt behandlet med 3–4 liter blod og Imizol (12 % w/v). De følgende år blev alle dyr på Hjortholm indfanget og behandlet med Imizol, ca. 4 uger efter de var sat på græs. Derefter stoppede udbruddene af babesiose, og kvægholderne havde lært ikke at indsætte naive dyr i et Babesia-endemisk område.
Dyr, der efterfølgende er født på øen, blev immuniseret, hvorfor antallet af kliniske tilfælde af babesiose var faldende i mange år, og der sås kun 2-3 tilfælde af blodpis. I perioden 1995-2000 ankom 20 RDM-stude, samt lidt Herefordkvier til Hjortholm. Der forekom ingen behandling eller dødsfald i den periode til trods for, at RDM-kvierne burde være naive, da de kom fra et Babesia-frit område.
På sydøen af Samsø ved Brattingsborg gods blev der i perioden 1985-1990 ligeledes observeret en død kvie med mistanke om babesiose. I 2008 var der endnu et udbrud af babesiose med dødsfald i en Limousine-besætning, som afgræssede nogle lavtliggende områder nord for Toftebjerg på Samsø, ikke langt fra Stavns fjord. Alle dyr blev herefter behandlet, og der forekom ikke flere dødsfald.
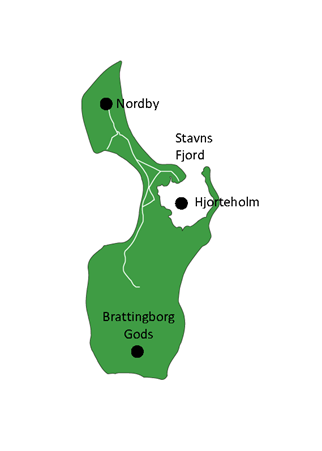
Kvægbestanden på Samsø har dog været faldende i en årrække, og det har resulteret i, at mange arealer ikke er blevet afgræsset. I 2017 blev en stor flok Limousiner og en mindre flok Hereford derfor sat ud i bakkerne i Nordby. Allerede to uger efter dyrene var ankommet, døde en Limousineko, og andre var klinisk påvirket med hæmaturi. Da babesiose er velkendt på Samsø, reagerede dyrlæge Lotte Christiansen fra Samsø Dyreklinik straks. DTU Veterinærinstituttet blev kontaktet, og der blev påvist Babesia divergens i alle de indsendte blodprøver. Der blev øjeblikkeligt igangsat behandling. Imidlertid døde yderligere to køer af babesiose.
Forløbet, som beskrevet her fra Samsø, er karakteristisk for udbrud af babesiose, når naive dyr indsættes i et endemisk område. Det understreger, hvorledes immuniserede kreaturer kan være smittebærere og få kliniske udbrud til at blusse op igen, når naive kreaturer indsættes i flokken.
DTU Veterinærinstituttet har gennem de sidste år fået flere henvendelser fra dyrlæger vedrørende mistanke om babesiose på kreaturer. Dyrlæger, som beskæftiger sig med kreaturer, bør derfor være opmærksomme på sygdommen.








